Se il via libera sarà approvato dalla Food and Drug Administration, entrerà in commercio la prima pillola contro il coronavirus.
Merck is seeking emergency-use authorization for its COVID-19 pill, putting it on course to become the first oral antiviral medication for the disease. (via @Reuters) https://t.co/MIxgx7tGBy
— Apple News (@AppleNews) October 11, 2021
La multinazionale Merck & Co., una delle più grandi società al mondo, ha chiesto il via libera all’immissione in commercio negli Stati Uniti della pillola antivirale contro il SARS-CoV-2. Lo ha annunciato questo lunedì 11 ottobre la stessa compagnia statunitense. Secondo quanto si apprende nella fonte ufficiale la casa farmaceutica ha richiesto l’autorizzazione alla Food and Drug Administration, l’ente governativo, dipendente dal Dipartimento della salute e dei servizi umani degli Stati Uniti d’America, che presiede al controllo e alla regolamentazione dei prodotti alimentari e farmaceutici sul mercato nazionale.
NON PERDERTI ANCHE >>> Almeno 16 morti nell’incidente aereo in Tatarstan: a bordo paracadutisti
Molnupiravir: farmaco efficace, ma non miracoloso
View this post on Instagram
TI POTREBBE INTERESSARE ANCHE >>> Liberata Suor Gloria Cecilia Narváez: quattro anni di prigionia
“Molnupiravir può diventare un farmaco importante nello sforzo globale contro l’emergenza pandemica.”, ha affermato il presidente di Merck Robert M. Davis. Il CEO della società statunitense ha confermato ai media la richiesta di autorizzazione all’agenzia farmaceutica americana (FDA): se la proposta del colosso farmaceutico statunitense sarà accolta, la pillola diventerà il primo farmaco antivirale disponibile sul mercato degli Stati Uniti d’America. Secondo l’ultima dichiarazione del produttore americano, il farmaco, sviluppato con la collaborazione dell’azienda biotecnologica Ridgeback Biotherapeutics, sarebbe un rimedio efficace nella lotta al coronavirus.
La pillola dimezzerebbe difatti il rischio di ospedalizzazione e morte, specie se somministrata pochi giorni dopo un test positivo. Il laboratorio ha annunciato il prosieguo dei test scientifici per accertare l’utilità del farmaco in termini di prevenzione dei casi di contagio. La sperimentazione clinica è stata condotta su un campione di 775 persone affette da coronavirus e ha dimostrato la parziale efficacia della pillola: “il 7,3% dei pazienti molnupiravir è stato ricoverato, contro il 14,1% dei pazienti placebo” Dall’analisi risulta evidente che il medicinale ha di fatto ridotto il rischio del 50%.
Tuttavia, la comunità scientifica ha alcune riserve. “Non è un farmaco miracoloso, ma uno strumento da accompagnamento alla campagna vaccinale.“, ha dichiarato su Twitter Peter Hotez, professore al Baylor College of Medicine di Houston.
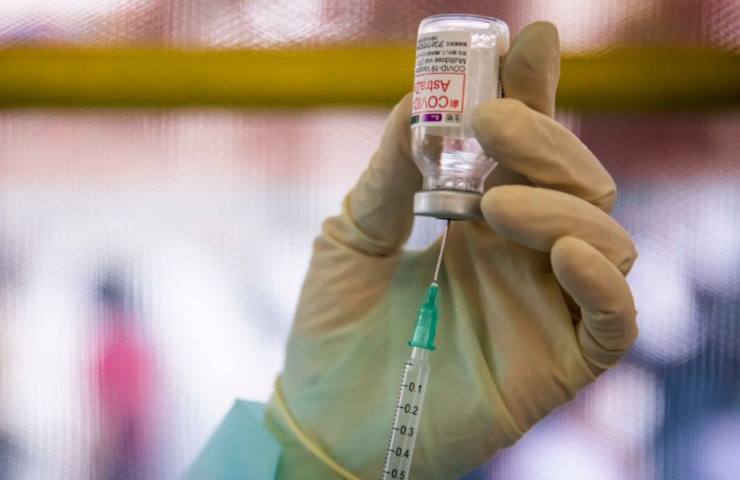
Altri esperti mettono in guardia anche sulla data di assunzione del trattamento, efficace solo se somministrato con ampio anticipo.
Fonte Nbc News